Vorgðnge bei einer Elektrolyse
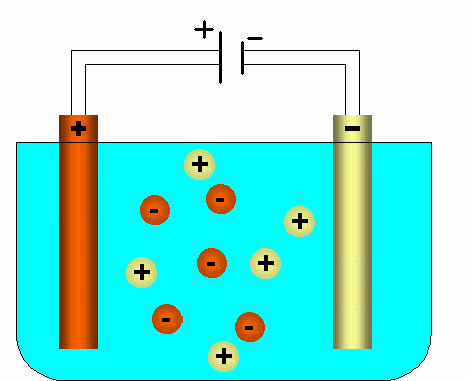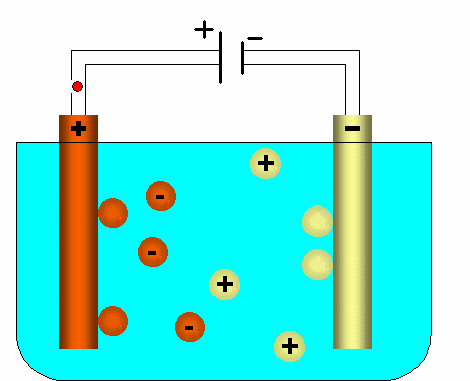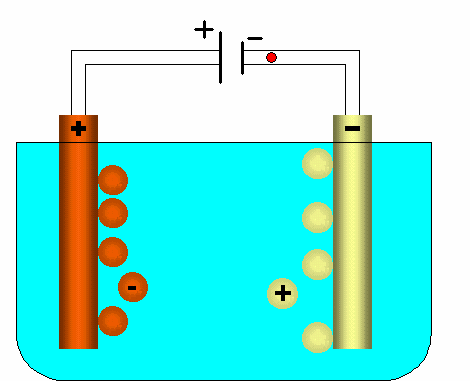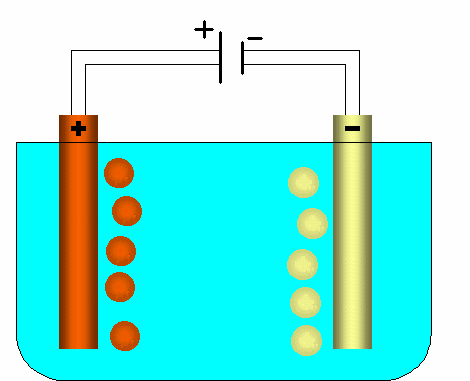
Elektrolyse von Salzl—sungen. Diese L—sungen enthalten negativ und positiv geladene Ionen (Anionen und Kationen).
Legt man nun eine ðuÔere Spannung an, so wandern die negativ geladenen Anionen zum positiven geladenen Stab in der L—sung.
Dort geben sie ihr/e Elektron(en) ab. Die Elektronen wandern weiter zum Pluspol der Spannungsquelle.
Die Kationen wandern zum negative geladenen Stab und nehmen dort Elektronen auf, die vom Minuspol der Spannungsquelle geliefert werden.
Die gesamte Anordnung stellt demnach einen geschlossenen Stromkreis dar.